No.04(2006.7)
カンジダベータグルカンは気道炎症を引き起こす

独立行政法人 国立環境研究所
環境健康研究領域
領域長 高野裕久
Hirohisa Takano,M.D., Ph.D.
抗癌剤、免疫抑制剤、HIV感染の増加等に伴い日和見感染症は増加しつつあり、真菌症の重要性がクローズアップされています。Candida Albicansは、 臨床の現場で最も多く経験される真菌のひとつであり、肺は真菌感染の主たる標的臓器です。しかし、肺の細菌感染症の病態は数多く研究されてきたのに対し、 肺真菌症の研究は比較的少ないというのが実態でした。これには、肺真菌症の病態モデルが確立していないということがひとつの問題でした。
グラム陰性菌壁の構成成分であるLPSは、内毒素として様々な生物活性を有しています。これによる肺傷害や全身性炎症反応は、前回までに紹介して きました。一方、真菌類ではβ1, 3-グルカン層(BG)が細胞壁の剛直性の中心的役割を果たしています。しかし、その生物活性や生体の防御機構に与える影響等は詳しくは検討されていませ んでした。最近Candida albicansの細胞壁を次亜塩素酸酸化によって部分分解し、細胞壁β1,3グルカンを可溶化(Candida solubilized cell wall beta-glucan: CSBG)することが可能となり、このin vitro(試 験管内)の生物活性が検討されてきました。1)ヒト末梢血単核球及び顆粒球からのIL-8産生、2)マウス腹腔マクロファージからのIL-6産生誘導、 3)LPS刺激によるマクロファージからのnitric oxide産生の増強、4)補体第二経路活性化、5)血管透過性亢進等が列挙されます。しかし、CSBGが動物個体に及ぼす影響は検討されていませんでし た。今回われわれは、CSBGを動物に経気道曝露し、その病原性を明らかにしました。
マウスを以下の3群に分けました。
- vehicle経気道曝露群(4 % DMSO加PBS: 0.1 ml / body )
- CSBG経気道曝露群( CSBG : 50 μg / body in vehicle)
- CSBGギ酸分解物経気道曝露群(FM: 50 μg / body in vehicle)
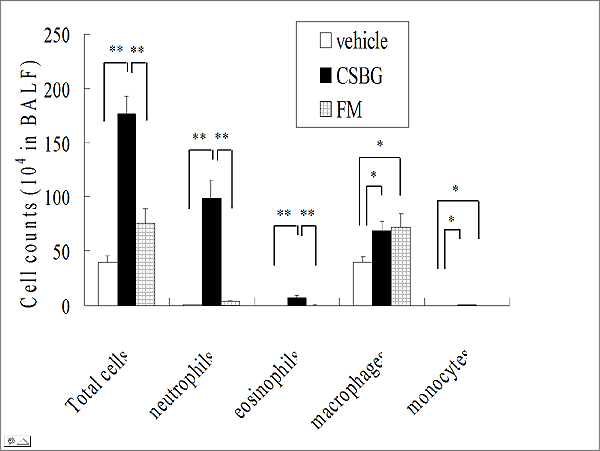
肺の病理組織学的所見、気管支肺胞洗浄液( BALF )中の炎症細胞所見、肺水分量、肺組織中サイトカイン濃度(IL-1β, TNF- α, KC ,MIP- 1α, MCP- 1 , eotaxin , RANTES , IL-5 ) 等を検討しました。
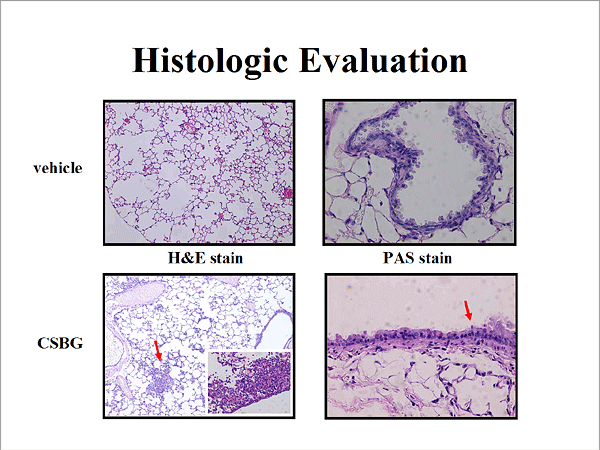
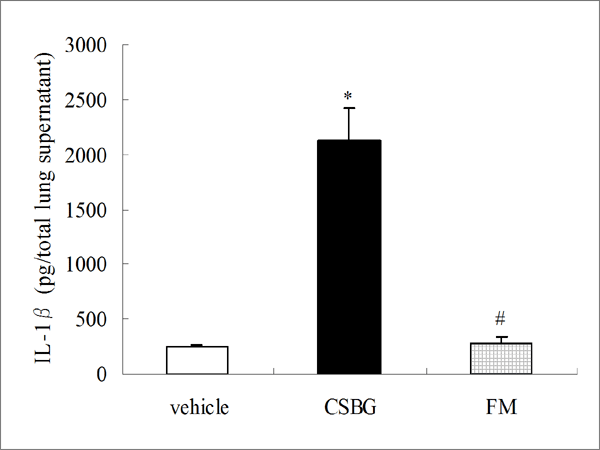
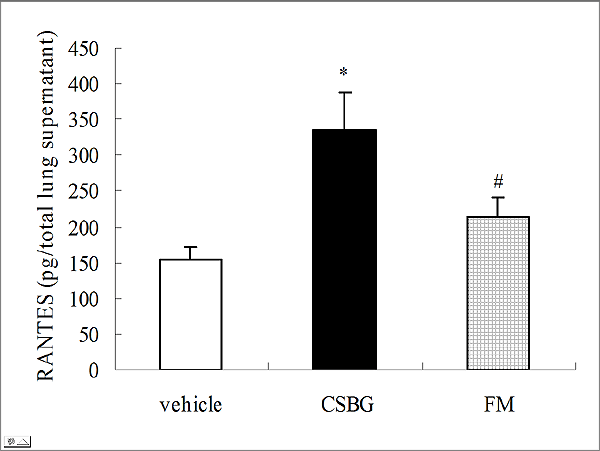
vehicle 曝露群と比較し、CSBG 曝露群では、炎症による有意な肺水分量の増加を認めました。同様に、CSBG 曝露群では、BALF中に好中球と好酸球が数多く浸出してきました(図1)。組織学的所見においても、CSBG 曝露群では著明な炎症細胞の出現と肺胞出血を認め、粘液を産生する細胞の出現も認めました(図2)。また、肺組織中では、主として好中球を活性化するIL-1β(図3)、 TNF-α、 KC,、MIP-1α、MCP-1やリンパ球、好酸球を活性化するRANTES(図4)やEotaxinが、 CSBG 曝露群で 、vehicle 曝露群と比較して有意に上昇していました。興味深いことに、ギ酸分解物曝露群では、これらの作用は非常に弱いものでありました。
今回の研究より、CSBGが呼吸器系に吸入されると、急性炎症が引き起こされることが明らかになりました。LPSはもっぱら好中球による炎症を引 き起こしますが、CSBGは、好中球とともに好酸球の浸潤や粘液産生細胞の出現も引き起こしてくることが大きな特徴でした。また、CSBGによる肺の炎症 は、局所の炎症性サイトカインやケモカインの上昇も伴っており、これが病態形成において重要であると考えられました。このあと、CSBGが炎症性タンパク の遺伝子発現に関わる転写因子に及ぼす影響を検討していますが、CSBGとLPSが活性化する転写因子は異なるようであり、病態の相違は、この相違に基づ く可能性が大きくなってきています。一方、ギ酸によるCSBGの分解が肺への影響をほぼ消失させることは、CSBGの構造及び分子量が炎症の誘導には重要 であることを物語っているものと考えられます。
われわれのモデルは、従来の真菌菌体を利用するモデルと比較して、1) 簡易である、2) contaminationを起こし難い、3) 均一性が保たれる、といった点で非常に優れていると考えられます。CSBGの経気道曝露モデルは、新たな肺真菌症の動物モデルとして大きな期待がかかります。
- 掲載内容は本情報掲載時点のものであり、予告なしに仕様、デザイン等を変更する場合があります。
- 表示の価格は、当社希望納入価格であり、消費税等は含まれておりません。